Типы батарей
Большинство современных аккумуляторных батарей – никель-кадмиевые, никель-металл-гидридные, а также все литиевые – были разработаны уже в 20-ом веке в лабораториях крупных компаний или университетов. Новые химические системы не изобретаются энтузиастами-одиночками, основывающимися на их собственной интуиции. Основные принципы, на которых основано функционирование батарей, уже досконально изучены и описаны точными формулами. Сегодня основные задачи, которые стоят перед разработчиками – это подбор оптимальных компонентов.

Химики различают гальванические элементы двух родов: первого и второго. Разница между ними заключается в том, как производится энергия, которую они вырабатывают.
Элементы первого рода – это одноразовые батареи, которые производят электроэнергию за счет химических реакций, в результате которых анод, катод и электролит претерпевают необратимые изменения. Это делает перезарядку таких батарей невозможной или очень нерациональной (к примеру, для зарядки некоторых типов батарей придется потратить в десятки раз больше энергии, чем они могут сохранить, а другие виды могут накопить только малую часть своего первоначального заряда). После этого батарею останется только выкинуть в мусорный ящик, откуда, как хотелось бы надеяться, она попадет в переработку (а скорее всего – на свалку).
Элементы второго рода чаще называют аккумуляторами. Это значит, что они могут заряжаться, если к электродам подключить источник постоянного тока. Химические реакции, протекающие в них, являются обратимыми. Таким образом, батареи второго рода не производят, а лишь сохраняют энергию.
При прочих равных аккумуляторы кажутся лучшим выбором по сравнению с одноразовыми батареями. Используя их, мы не наносим столько вреда окружающей среде, ведь после разрядки их не нужно выбрасывать. Один аккумулятор можно использовать около года, а обычных батареек на этот же срок понадобилось бы штук 100-200, и в каждом элементе содержатся токсичные вещества. Но не все так просто. На деле аккумуляторы имеют несколько серьезных недостатков, которые не позволяют им вытеснить все остальные батареи. В случае срочной необходимости одноразовые батарейки являются лучшим выбором. Они дешевы и всегда готовы к работе. Но для мобильных устройств, используемых регулярно, аккумуляторы продолжают оставаться наиболее выгодным вариантом.
Ни одна батарея не может хранить энергию вечно. Химические вещества внутри реагируют между собой и постепенно разлагаются. В результате снижается заряд батареи. У этой постепенной разрядки есть две основные причины.
Некоторые химические реакции влияют на способность хранить энергию. Через некоторое время батарея потеряет весь свой заряд. Этот промежуток времени, называемый сроком хранения, обычно указывается на ее корпусе. Он зависит от типа и конструкции батарей, но условия хранения также влияют на продолжительность их жизни. Современные литиевые батареи могут храниться более десяти лет, в то же время элементы других типов могут разрядиться за пару недель (к примеру, цинк-воздушные батареи после начала использования). Но даже самые «долгоиграющие» образцы могут прийти в негодность гораздо раньше, если они будут храниться в неблагоприятных условиях. Особенно сильно сказывается влияние высоких температур. Если же их, наоборот, охладить (а некоторые типы даже заморозить), то это часто помогает сохранить их в лучшем виде на время, значительно большее указанного срока годности.
Обратимые химические реакции в аккумуляторах протекают даже тогда, когда они не используются. Этот процесс называется саморазрядкой. Он является обратимым, также как и обычная разрядка. На скорость саморазрядки влияют те же факторы, что и на срок хранения, поэтому она также может сильно отличаться у разных типов батарей: одни теряют до 10% заряда в день, а другие лишь 1%.
Еще один показатель, который важно знать для каждого типа батарей, это удельная емкость. Она определяется как отношение энергии элемента к его массе или объему и выражается в Ватт-часах на единицу массы или объема
Чем выше этот коэффициент, тем больше энергии может храниться в единице веса, и тем более привлекательна она для использования в переносных устройствах. В этой таблице приведены отношения для различных типов аккумуляторов, выраженные в Вт-ч/кг.
| Тип | Вольтаж | Уд. емкость |
|---|---|---|
| Ni-Cad | 1,2 | 40 – 60 |
| NiMH | 1,2 | 60 – 80 |
| Li-Ion | 3,6 | 90 – 110 |
| Li-Polymer | 3,6 | 130 – 150 |
Чем отличаются солевые батарейки и щелочные
Солевые и щелочные батарей отличаются составом. И состав и делает разницу между двумя типами источников питания солевыми и щелочными. Щелочные имеет внутри цинк, калий, марганец и латунный стержень которой и контролирует токоотвод.
Щелочные батарейки.
Солевые батарейки — что это такое: состав и характеристики
Солевые батареи самые дешёвые из аккумуляторов. В аккумуляторах используют цинк, графит, марганец. Для отрицательного заряда используют цинк с графитом, а для положительного двуокись марганца. Электролита сделана из хлорида аммония.
Популярность в народе солевые батарейки приобрели с помощью своей дешевизны в сравнении с щелочными. Также солевые накопители делают почти всех форматов, что и позволяет им бить на плаву.
Разница в маркировке
Разница с солевой и щелочной батарейкой не только в составе, но и по маркировке. Маркировка солевой и щелочной выражается солевая маркируется «R», щелочная «LR». Также могут бить другие маркирование которые будут значить точный состав батарейки например «SR», «CR», «PR» значит что в аккумуляторе, содержаться серебряно-цинковые метали или другие.
Преимущества и недостатки соляных батареек
Преимущество солевых аккумуляторов в их цене и в малом весе изделия. Солевые источники питания менее токсичны, но утилизировать их нужно.
Недостатки в сроке службы не более 3 лет. При неправильном хранении то возможна протечка или высыхания элементу и после этого батарейка не сможет работать. Также в плохое соотношения ёмкость с весом изделия. Солевые накопители много чем уступают щелочным, но их будут покупать через доступность.
Солевые элементы питания.
Классификация батареек по типоразмеру
Как известно многие элементы питания имеют разную форму. Специально поэтому была разработана маркировка батареек согласно их виду. Имеется европейская и американская классификация.

Ниже приведена таблица в которой отображаются источники энергии по типоразмеру. Она поможет определить тип батарейки.
| Американская маркировка | Народная маркировка | Кодированные обозначения | По типу | Ширина в мм | Высота в мм | Емкость в mAh. |
| А | нет | LR23R23 | Щелочная Солевая | 17 | 50 | Не известно |
| АА | Пальчиковая | FR6LR6R6 | Литиевая Щелочная Солевая | 14.5 | 50.5 | 1100 – 3500 |
| ААА | Мизинчиковая | LR03FR03R03 | Щелочная Литиевая Солевая | 10.5 | 44.5 | 540 – 1300 |
| АААА | Маленькая мизинчиковая | LR8D425 | Щелочная | 8.3 | 42.5 | 625 |
| В | LR12 | Щелочная | 21.5 | 60 | 8350 | |
| С | Средняя | 26.2 | 50 | 3800 – 8000 | ||
| D | Большая, круглая | LR14 R14 | Щелочная Солевая | 34.2 | 61.5 | 8000 – 19500 |
| F | LR20R20 | Щелочная Солевая | 33 | 91 | неизвестно | |
| N | LR1R1 | Щелочная Солевая | 12 | 30.2 | 1000 | |
| ½ AA | R14250 | Солевая | 14.5 | 25 | ||
| R10 | 21.5 | 37.3 | 1800 | |||
| PP 3 | Крона | 1604, 6F22, 6R611604A, 6LF22, 6LR61, MN1604, MX1604 | Солевая Щелочная | 26.5 | 48.5 | 150 – 1000 |
| А 23 | Мини мизинчиковая | ANSI-1181A, 8LR23, 8LR932, GP23A, E23A, LRV08, MN21, V23GA | 10.5 | 28.9 | 40 |
На этикетке элемента питания можно заметить американскую маркировку. Так же там указывают из чего она состоит, а также проставляют дату. Значение L на батарейке указывает на то, что она щелочная. Размеры от указанных могут слегка отличаться. Например, если батарея находится в плотной этикетке, то ее габариты будут на 1-3 мм больше. Такую оболочку производитель ставит чтобы защитить источник энергии от погодных условий и ударов при падении.
Стандартные обозначения по IEC
| Обозначение | Тип энергетического источника |
| PR | Воздушно цинковые |
| R | Солевые |
| CR | Литиевые |
| SR | Серебряные |
| LR | Щелочные |
Таким образом виды гальванических элементов могут быть разными.
Химические процессы внутри батарейки
Коротко о происходящем внутри металлического корпуса. Электрические батарейки состоят из двух частей, катода и анода, и жидкости или геля, заполняющего корпус, по совместительству выполняющий роль корпуса и резервуара. Жидкость называется электролитом и обладает некоторой химической активностью. Активность специфическая — электролит забирает электроны на одном полюсе (катод), и отдает их на другой (анод). Там, где избыток электронов, получается заряд «минус», там, где дефицит — «плюс».
По типу электролита и материалов анода и катода, батарейки подразделяются на:
- Солевые. Узнать их можно по маркировке R. Электролит — хлорид аммония. Катод — цинк, анод — кальций. Это самые дешевые батарейки с небольшим запасом работоспособности.
- Щелочные. Маркировка LR. Часто пишут также слово Alkaline. Электролит — гидроксид натрия или калия, катод — цинк, анод — оксид марганца. Обладают средней работоспособностью, но намного лучше солевых. Щелочные батарейки способны создавать напряжение до 12 В, но в быту используются стандартные, на 1,5 В. Так удобнее.
- Литиевые. Маркировка CR. Отличаются тем, что при разной нагрузке выдают стабильный ток. Используются, преимущественно, в точной электронике.
- Серебряные. Маркировка SR. Анод цинковый, катод серебряный. Отличаются высокой емкостью и значительным сроком службы. Используются в дорогой технике, например, хороших наручных часах.
Также выпускаются ртутные батарейки, но по причине токсичности жидкого металла, в бытовой технике практически не используются. Применяются преимущественно в специальных приборах, рассчитанных на эксплуатацию при низких температурах.
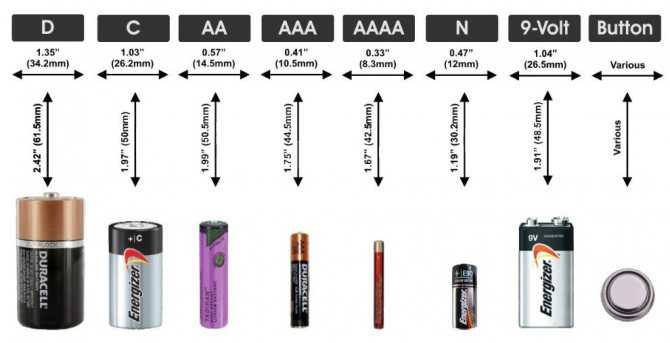
Размеры батареек
Самые распространённые батарейки для игрушек, карманных фонариков, настенных часов, беспроводных клавиатур и мышей — это то, что мы привыкли называть словами «пальчиковые» и «мизинчиковые».
Пальчиковые батарейки маркируются латинскими буквами AA или LR6. Имеют номинальное напряжение питания 1,5 В. Размеры: длина 50,5 мм, диаметр 14,5 мм.
Ёмкость, которая влияет на срок активной службы, зависит от начинки: солевые или алкалиновые. Разумеется, алкалиновые гораздо круче по всем параметрам, кроме цены.
Мизинчиковые батарейки маркируются как AAA. Часто их используют как замену большим элементам питания напряжением от 3,7 до 4,5 В, комбинируя по три штуки. Но применяют и по отдельности.
Кроме этих двух типоразмеров имеется масса других, менее распространённых. С разными характеристиками и разным напряжением.
Виды батареек по химическому составу
Наиболее часто функции источников напряжения выполняют цинково-марганцевые и литиевые составы. Существуют и другие типы элементов питания.
Солевые
Изделие такого типа стоит недорого, что объясняется низкой энергоемкостью. Элемент имеет разные размеры. Принцип работы основывается на вступлении диоксида марганца в химические реакции. Цинк выступает в роли анода и корпуса. Проводит ток хлорид аммония, находящийся в распределительных отверстиях. Вещество представляет собой вязкую субстанцию. Солевые батареи используются для питания устройств, потребляющих небольшое количество энергии.
Конструкция солевой батарейки.
К преимуществам таких элементов относятся:
- низкая стоимость;
- простая конструкция;
- удобство в применении;
- возможность использования в бытовых условиях.
Отрицательными качествами считаются:
- чувствительность к перепадам температур;
- небольшой срок хранения;
- быстрая потеря заряда;
- невозможность повторной зарядки;
- высокий риск утечки солевого компонента.
Серебряные элементы
Конструкция включает серебряный катод, цинковый анод и электролитный состав. Принцип действия аналогичен с таковым у ртутных элементов. Серебряные батарейки устанавливаются в наручные часы.
Конструкция батареек кнопочного типа.
Их отличают такие особенности:
- бесперебойная работа при низких температурах;
- подача высокого напряжения;
- увеличенная емкость.
Батарейки не утрачивают заряд при длительном хранении. Единственным недостатком считают высокую стоимость.
Щелочные или алкалиновые
Алкалиновыми называются источники, где электрическое напряжение возникает за счет преобразования вязкого гидроксида кальция. Цинковый анод пребывает в порошкообразном состоянии. Катод производится из диоксида магния. Материал устойчив к коррозии, что помогает продлить срок службы батареи.
Конструкция алкалиновой батарейки.
По сравнению с солевыми элементами алкалиновые имеют большую емкость. Они могут использоваться при низкой температуре. Их применяют люди, занимающихся строительством, поиском металла, плаванием.
Ртутные батарейки
В прошлом ртутные источники питания устанавливались в фотоаппараты, космические и военные приборы. Элементы содержат ртутно-цинковый состав. Для улучшения характеристик батарейки электроды покрывают серебром и гидроксидом магния.
К преимуществам относят нечувствительность к изменению температур, возможность восстановления заряда. Источники выдают постоянное напряжение и служат не менее 2 лет.
Литиевые
Существует 3 разновидности литиевых батарей:
- С твердыми катодами. Эти части аккумулятора состоят из лития. В качестве анода используются сульфиды или оксиды. Напряжение достигает 1,5 В. Устройства применяются часто, что объясняется нечувствительностью к перепадам температур, высокой емкостью и низкой потерей заряда.
- С жидким окислителем. Источником напряжения является диоксид серы, погружаемый в вязкий раствор тионилхлорида. Катоды представляют собой алюминиевые пластины с углеродистым напылением. Бромид лития выступает в роли проводника электричества. При установке в мощные устройства батарея быстро разряжается. Некоторые элементы питания содержат токсичные вещества или взрываются при неправильной эксплуатации.
- С йодом. Вещество является окислителем, литий – восстановителем. Заряд сохраняется в течение длительного времени. Батарейки используются для поддержания работы кардиостимуляторов.
Необычные типы батареек
A.
Имеют форму цилиндра. Относятся к щелочному типу. Напряжение 1.5 вольт. По маркеровке IEC носят название R23. Габариты 17 на 50 мм. Раньше использовались в нестандартных устройствах и стареньких компьютерах. На данный момент их практически не найти.
AAAA.
Именуются как LR61. Являются очень миниатюрными щелочными элементами питания цилиндрической формы. Напряжение 1.5 V. Габариты 8,3 на 42.5 мм. Такие длинные батарейки используют в фотоаппаратах, фонариках, мощных стилусах, лазерных указках, глюкометрах.

B.
Являются солевыми и маркируются как R12. Есть так же щелочные с обозначением LR12. Выполнены в виде цилиндрической формы. Размер 21,5х60 мм. Напряжение 1.5 вольт. Часто используют в осветительных установках.
F.
Имеют напряжение 1.5 V. Именуются как L25 и LR25. Производители выпускают солевые элементы с энергетической емкостью от 10,5 mAh и щелочные до 26 mAh. Габариты 33х91 мм.
N.
Маркируются как R1 и LR1. Емкость 400-1000 мАч. Напряжение 1.5 V. Габариты 12х30,2 мм.
1/2AA.
Имеют обозначение CR14250. Тип Li‑MnO2 (литий-диоксид марганцевые). Вольтаж 3,6 V. Li‑SOCl2 (литий-тионил хлоридные) маркируются как ER14250. Параметры 14х25 мм.
R10.
Вольтаж 1.5 вольт. Производство запущено еще в Советском Союзе. Имеют по мимо основные маркировки еще и как 332. Размер 21 на 37 мм. На данный момент их производство снижено.
Есть схожие батареи, имеющие внутри 2 элемента R10. Такой источник тока имеет маркировку 2R10 и габариты 21,8х74,6 мм. Его вольтаж равен 3 V. Именуются он как Duplex.
A23.
Имеет повышенное напряжение 12 v. Ее габариты равны 10,3х28,5 мм. По типу она щелочная. По стандарту IEC маркируется как 8LR932. При вскрытии обнаруживается обычно 8 батареек типа LR932 соединенных друг за другом. Используется чаще всего в пультах ДУ и игрушках.
A27.
Стандарт IEC — 8LR732. Тип щелочной. Размеры 8х28,2 мм. Вольтаж 12 V. Так же, как и предыдущая имеет внутри последовательное соединение восьми батарей типа LR632. Требуется для радио пультов, зажигалок, сигарет, работающих от электричества.
3336.
Маркируется по IEC как 3LR12 и имеет щелочной тип. А 3R12 является солевой. Люди называют их квадратными так как у них прямоугольная форма. Производят подобные источники тока с 1901 года. Тогда они использовались только в фонариках. Через некоторое время их стали применять в радиоприемниках, датчиках влажности, игрушках и других устройствах. Напряжение у них 4.5 вольт. Энергоемкость 1200 – 6100 mAh. Габариты 67х62х22.
По сути это три соединенных последовательно пальчиковых батарейки R12.
На данный момент в продаже имеются разные виды батареек. Поэтому вы без труда сможете подобрать нужную именно вам! Лучше всего брать элементы питания уже проверенные временем. Либо же приобретать источники тока от известной компании.
Корпус для батареек и из чего он сделан
После ознакомления с тем, как устроен аккумулятор телефона, остается ознакомиться с корпусом этой детали.
Он состоит их двух слоев:
- Верхний слой. Пластиковое покрытие. Изолирует банку батареи, защищает ее от воздействия внешних факторов. Еще на покрытии производитель печатает информационный блок.
- Внутренний слой. Это – металл. Материал твердый и прочный, защищает внутренности от повреждений.
Производители аккумуляторов для техники используют металл с определенным показателем эластичности. Это делается для того, чтобы корпус выдержал деформации в случае вздутия батареи.
Принцип работы батарейки
Принцип работы батареи довольно прост для понимания. Схема образования электричества выглядит следующим образом:
- Цинковый стакан элемента питания в результате химической реакции приобретает отрицательный заряд.
- Графитовый стержень становится положительно заряженным.
Отрицательные ионы, которые поступают на соответствующий вывод, потекут к положительному полюсу при подключении какой-либо нагрузки, например, лампочки или моторчика.
В общем, устройство батарейки представляет собой очень простую схему, которую, при желании, можно повторить самостоятельно в домашних условиях, используя при этом вполне доступные химикаты и металлические изделия.
Особенности химического состава
В зависимости от веществ, которые используют внутри батареи, такие изделия могут быть солевыми, щелочными или литиевыми. Каждая группа имеет свои особенности химического состава.
Солевой
В качестве катода в солевой батарее используется цинк, а анод представляет собой стержень, изготовленный из графита и MnO2. Электролит в элементе этого типа – это хлорид аммония или калия. Для придания необходимой консистенции в него также добавляют специальный загуститель.

Элементы питания этого типа, в которых в качестве анода используются серебро, обладают значительно большим сроком годности. Называются такие элементы серебряно-цинковыми и стоят значительно дороже простых солевых батареек.
Щелочной
Строение алкалиновой батарейки практически не отличается от солевой. Разница заключается только в том, что в щелочном элементе серединный стержень устанавливается на отрицательный вывод, а не на положительный.
Химический состав изделия этого типа следующий:
- Катод – диоксид марганца.
- Анод – порошкообразный цинк.
- Электролит – гидрооксид калия.
Основное преимущество марганцево-щелочных элементов перед солевыми батареями заключается в большей ёмкости.
Литиевой
Литиевые неперезаряжаемые элементы имеют следующий химический состав:
- Анод – литий или литиевые соединения.
- Катод – диоксид марганца, пирит и другие.
- Электролит – перхлорат лития, тионилхлорид.
Литиевые элементы питания работает в различных устройствах значительно дольше щелочных и солевых изделий, но и стоимость их на порядок выше.
Маркировки батареек
Согласно стандарту IEC (Международная электротехническая комиссия), маркировку гальванических источников тока делают исходя из состава электролита и активного металла, применяющихся в их конструкции.
По этой классификации существует 5 самых распространенных типов круглых (цилиндрических) батареек: солевые, щелочные, литиевые, серебряные и воздушно-цинковые. Буква R в их обозначении означает круглую форму (от английского round).
Солевые батарейки (R). Имеют катод из цинка, анод из диоксида марганца и электролит из хлоридов аммония и цинка. Они обеспечивают напряжение 1,5 вольта, имеют небольшую емкость, высокий саморазряд и низкий срок хранения (до 2-х лет). При низких температурах они неработоспособны.
Солевые батарейки самые дешевые и имеют посредственные технические характеристики. В обиходе их также называют цинк-карбоновыми и угольно-цинковыми.
Литиевая и Щелочная батарейка
Щелочные батарейки (LR). Имеют катод из цинка, анод из диоксида марганца и электролит из гидроксида щелочного металла. Они имеют напряжение 1,5 вольта, увеличенную емкость, низкий саморазряд и большой срок хранения до 10 лет. Они сохраняют работоспособность при низких температурах до -20 градусов.
Эти источники тока недороги, в обиходе их еще называют алкалиновыми и щелочно-марганцевыми.
Литиевые батарейки (CR). Имеют катод из лития, анод из диоксида марганца и органический электролит. Они имеют напряжение 3 вольта, большую емкость, малый саморазряд и большой срок хранения до 10-12 лет. Они сохраняют работоспособность при низких температурах до -40 градусов. Эти источники тока довольно дороги.
Серебряные батарейки (SR). Имеют катод из цинка, анод из оксида серебра и электролит из гидроксида щелочного металла. Они имеют напряжение 1,55 вольта, высокую емкость, малый саморазряд и длительный срок хранения до 10 лет. Они сохраняют работоспособность при низких температурах до -30 градусов. Как правило, применяются в часах. В обиходе их также называют серебряно-цинковыми.
Воздушно-цинковые элементы (PR). Имеют катод из цинка, анод из кислорода и электролит из гидроксида щелочного металла.
Эти источники тока являются самыми чистыми с точки зрения экологии, благодаря чему широко используются в специальных медицинских устройствах, но имеют самый малый срок эксплуатации (несколько недель после вскрытия упаковки). Они имеют среднюю стоимость, имеют напряжение 1,2-1,4 вольта и очень высокую емкость (больше, чем у литий-ионных элементов в 2-3 раза), сохраняют работоспособность при температурах от -20 до +35 градусов.
История создания
В 1867 году Джоржес Лекланше изобрёл первую вариацию химического источника тока. Первая батарейка сильно отличалась внешним видом по сравнению с современным аналогом.
Однако идея о накоплении электричества была представлена впервые в разработке А. Вольта, большинство людей на вопрос, о том, кто придумал батарейку, называет именно его. Компания Everedy стала первой производить автономные источники питания для шахтёров. Позже устройством начали пользоваться люди, уходившие в дальние плавания.
Большой шаг в процессе развития батареек постоянного тока сделала компания Duracell, выпускавшая дешёвые и компактные виды источника питания. В стакане из цинка помещался графитовый стержень, находящийся в оксиде марганца. До середины XX века этот тип и принцип работы батарейки оставался неизменным.
Открытием стало изобретение литиевых аккумуляторов. В них накапливалось большее количество энергии, чем у предшественников. С течением времени источники претерпели огромное количество изменений. Имеется множество вариантов того, как устроена батарейка.
Что внутри батарейки?
Ниже будет рассмотрено строение четырех типов источников питания. По сути принцип работы один и тот же, но состоят эти энергетические накопители из разных составляющих.
Состав пальчиковой батарейки
В состав батареи входят следующие элементы:
- Катод – это отрицательный полюс
- Вкладыш служит некой прокладкой
- Диафрагма
- Футляр
- Электролит – жидкость вследствие которой идет химическая реакция
- Стержень сделанный из угля
- Крепежная шайба
- Анод или положительный полюс
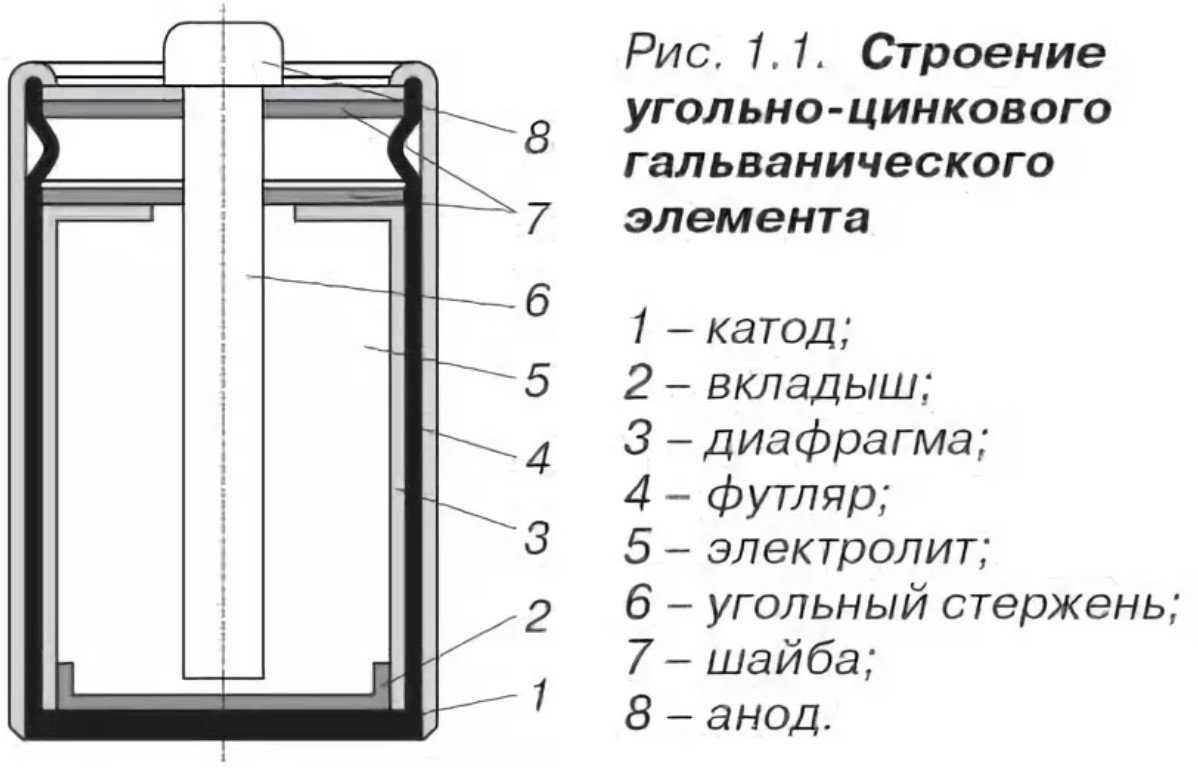
Примерно так выглядит состав батареек пальчиковых. Но иногда их устройство бывает иным. Например, в строение может быть использован лишь угольный стержень, специальный темный порошок и металлические элементы.
Устройство круглой батарейки
Приплюснутый элемент питания имеет своеобразную форму. Вот строение батарейки в разрезе:
- Положительный торец
- Отрицательный полюс
- Пористая прокладка, вымоченная в электролите
- Оксид ртути
- Порошок Zn
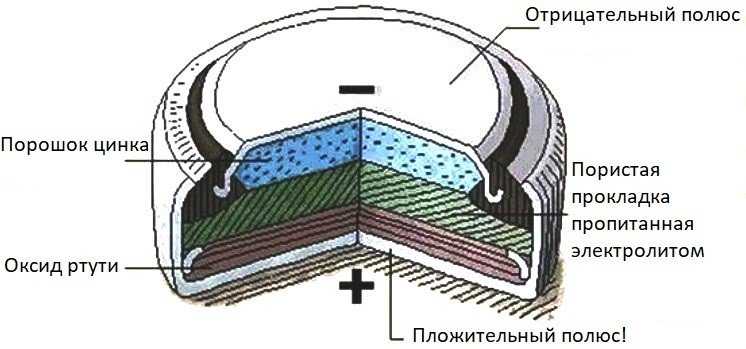
Устройство батарейки может быть и немного иным:
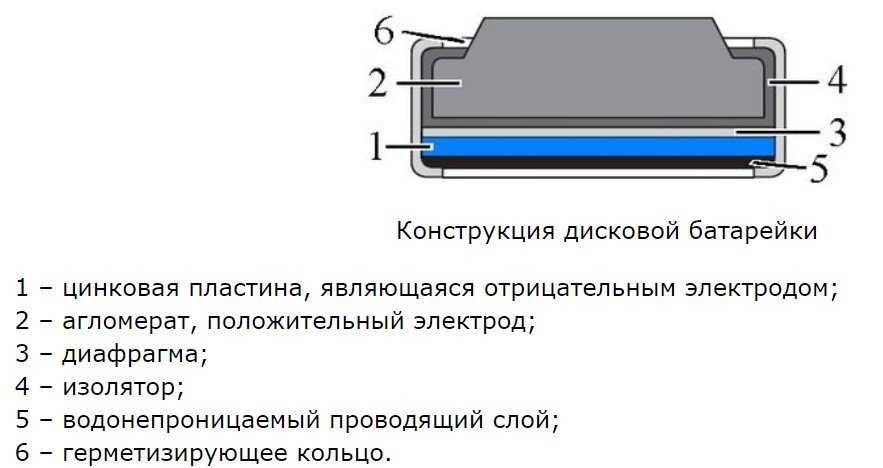
Детали энергетического элемента:

Если сильно нагреть данный эелмент, то под напором внутреннего газа она запросто может взорваться. Таким образом сейчас вы можете созерцать что внутри у батарейки.
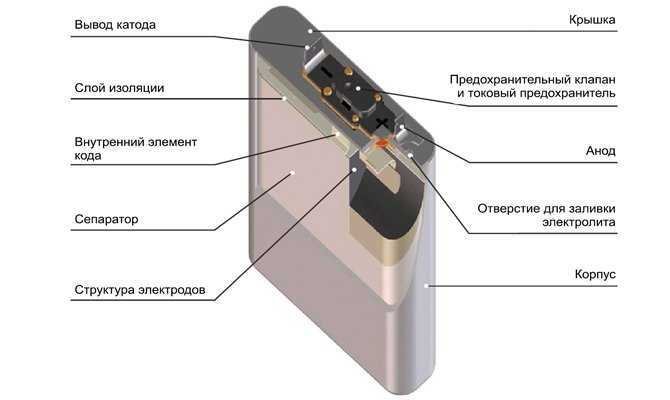
Устройство батареи телефона
Принцип устройства батарейки мобильника:
- Положительный и отрицательный полюс
- Анодный стакан
- Катодный контакт
- Сепаратор
- Уплотнение
- Защитный клапан
- Изолятор
- Колпачок
- Перегородка
- Корпус алюминиевый или иной
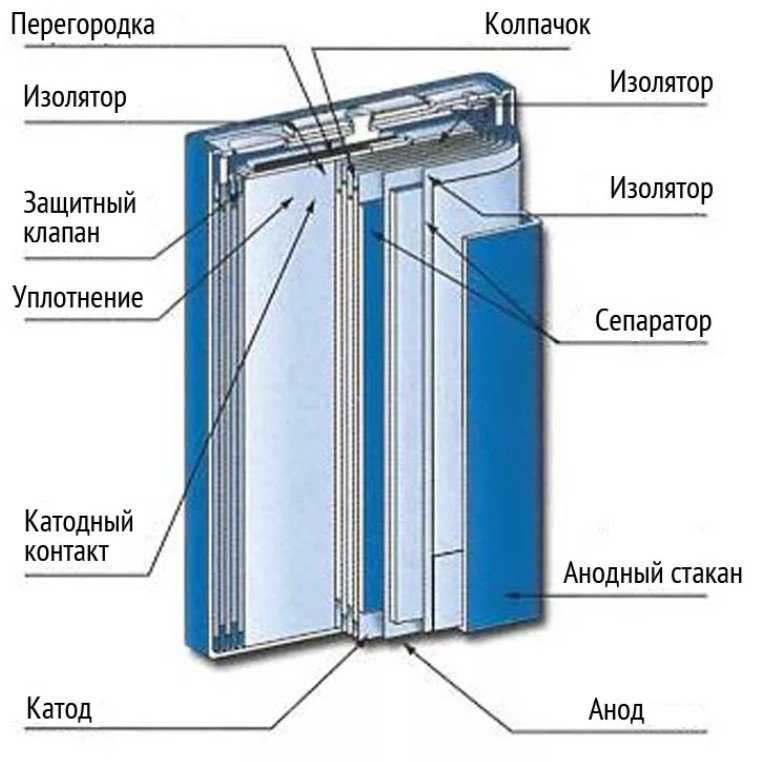
Таким образом устройство батарейки мобильного телефона немного сложнее обычного солевого источника питания.

Из чего состоит батарейка Крона?
Данный источник энергии устроен следующим образом. Контакты плюс и минус находятся друг на против друга в верхней части элемента питания. Под ними расположена пластмассовая основа. От отрицательного контакта идет пластина на минусовой полюс. И там она плотно прикрепляется. Состав батарейки схож с выше приведенными источниками питания.
Внутри металлического прямоугольного стаканчика находятся 6-ь закругленных сплющенных прямоугольников. Каждый из которых является отдельной батареей. Размер данных элементов: Длинная: 2,2 см; Ширина 1,5 см; Высота: 0,5 см. Каждый такой бочонок имеет заряд 1,5 вольта. Друг от друга они отделены специальными пластинами. Но все же они соединены между собой в середине. Подобное устройство батарейки экономически выгодно!
Что находится внутри батарейки крона?
Вот собственно батарейка в разрезе. Иногда она может быть такой.


Но обычно можно заметить, что крона выполнена по такому типу как на рисунки ниже.



Ее строение достаточно простое:
- 2 контакта «+» и «-».
- Металлический корпус.
- Нижняя и верхняя пластины, выполненные из пластика.
- Шесть прямоугольников на 1,5 вольта соединенных между собой.
- Электролит.
- Угольный стержень
- Внутренняя пленка.
- Изоляционные пластины.
- Устройство батарейки включает в себя так же обертку.
Устройства
Большая часть устройств предполагает использование батарей одного из стандартных размеров, например, AA, AAA и тому подобное. Поэтому у покупателей есть выбор, элементы какого типа предпочесть.
Надпись»Heavy-duty» (высокая нагрузка), которую можно увидеть на некоторых угольно-цинковых батарейках – не просто рекламный ход. Это означает, что они предназначены для использования в устройствах, нуждающихся в токе большой силы. Пример таких устройств – фонари, электромоторы и все приборы, в которых они применяются, например детские игрушки. Там эти батареи прослужат гораздо дольше, чем обычные. Если же прибор потребляет мало электроэнергии, то преимущество почти будет почти незаметно.
Разные литий-содержащие батарейки сильно отличаются друг от друга в том, что касается области применения. Литий-железодисульфидные являются рекордсменами при работе с большими нагрузками. Другие типы, например литиевые часовые батарейки, применяются там, где нагрузки, наоборот, не велики. Литий-ионные и литий-полимерные находятся где-то посередине, а потому являются наиболее универсальными.
Там, где могут быть использованы и аккумуляторы, и одноразовые батарейки, предпочтительнее обычно оказываются первые. Но в некоторых случаях их преимущества бывают не востребованы. Возьмем, к примеру, пульт дистанционного управления, который потребляет очень мало энергии, но используется постоянно и на протяжении длительного времени. Обычные батарейки могут прослужить в нем несколько лет, а аккумуляторы вообще столько не живут, к тому же на таких длительных промежутках времени дает о себе знать гораздо более высокая скорость саморазрядки этих элементов. На другом полюсе находятся устройства, которые используются редко, но должны быть всегда готовы к работе в случае необходимости. В них тоже лучше поставить что-нибудь одноразовое, но «долгоиграющее». В общем, принцип понятен – нет самой лучшей батареи или аккумулятора, для каждого конкретного применения что-то будет хорошо, а что-то плохо.
Напоследок повторим несколько важных правил:
Если какой-то металлический предмет закоротит контакты батареи, то она начнет нагреваться. Это может вызвать порчу вашего имущества и даже пожар.
Большинство аккумуляторов вырабатывает водород в процессе электролиза, вызванного перезарядкой. Герметизация корпусов современных батарей значительно уменьшает риск утечек и возгорания газа, но полной гарантии никто дать не может, потому что встроенные клапаны периодически выпускают излишки скопившегося водорода.
Гораздо большую опасность несет газ, который не может покинуть корпус. Если по какой-то причине автоматические клапаны оказались заблокированы, при повышении температуры давлении внутри может вырасти настолько, что батарея взорвется. Поэтому корпус аккумуляторов никогда не должен заклеиваться, запаиваться в пластик и тому подобное.
Почти все батареи содержат опасные химические соединения: токсичные, ядовитые, легковоспламеняющиеся – это зависит от технологии
Поэтому важно, чтобы они были правильно утилизированы после использования. Понятное дело, что все равно все это окажется на ближайшей свалке, но уж лучше пусть они лежат где-нибудь далеко, чем валяются на улице.
Статья опубликована на сайте HPC.RU.Перепечатывается с разрешения редакции.
Что внутри батарейки?
Самые сложные элементы аккумуляторов мобильников находятся внутри корпуса. Можно изучить их конструкцию и основные функции. Кроме банки с ионами лития и сепаратора, конструкция оснащена контроллером.
Контроллер – это «мозги» батареи сотового, состоит из таких элементов:
- Резисторы (в схеме питания, защиты).
- Терморезистор.
- MOSFET-транзисторы.
- Микросхема.
- Конденсатор накопления.
Контроллер выполняет следующие функции:
- Контроль заряда. Аккумуляторы телефонов заряжаются постепенно. Первых 10% с невысокой скоростью, потом ускорение до 80%, и конечный этап – замедление. С высокой скоростью заряжается лишь «средняя часть» батарейки, такая особенность работы для снижения нагрузки.
- Защита от перезаряда. Ток от сети поступает, но при достижении напряжения в 4,2 В питание автоматически останавливается.
- Защита от разряда. Установлено и минимальное напряжение, на уровне, примерно в 2,9 В. Даже если процент упал до 0, и мобильный телефон выключился, в аккумуляторе остается небольшой запас. Если его не будет – потеряется полезная емкость.
- Ограничение тока. Напряжение не всегда стабильно, великие скачки или короткое замыкание – однозначно повредят батарею. Это плохо скажется на длительности срока эксплуатации. Ограничитель препятствует этому.
- Балансировка батареи. Это конструкция, состоящая из последовательных электронных элементов. Такая схема обеспечивает равномерный заряд разных частей. От функции зависит долговечность батарейки.
- Контроль за температурой. В каждой батарейке установлен терморезистор. Он контролирует температуру и при надобности защищает устройство от перегрева или переохлаждения.


































